酶和一般化學催化劑一樣,它參與化學反應,但反應前后沒有質和量的變化,也不改變可逆反應的平衡點。醇和一股化學催化劑不同,酶是蛋白質,它兼有生物大分子的各種特性。
酶促反應的“中間產物”學說:
在酶促反應中,人們稱反應前的反應物為底物、反應后為產物。
酶(E)首先與底物(S)生成中間產物——“酶-底物復合物(ES)”,然后這復合物再分解成產物(P)和游離的酶(E)。其過程如圖二所示
|
|
| 圖二 雙底物酶促反應示意圖 |
(一)酶促反應的特性
(1)酶有極高的催化效率
一般情況下,酶的催化效率比非催化反應高108-20倍,比非酶催化反應高107-13倍。
在化學反應中,只有當碰撞的分子能量等于或超過某一定的能量Ec(活化能)的活化分子時,才是有效碰撞,才發生化學反應。使分子從常態轉變為容易發生化學反應的活躍狀態所需要的能量稱為活化能。如圖三所示
|
|
| 圖三 酶促反應過程中活化能的改變 |
酶促反應速率也與其活化能的大小密切相關,活化能越低,反應速率越快,因此降低活化能會有效地促進反應的進行。
(二)酶促反應的特異掛
除了酶促反應能在很溫和的條件下順利和高速進行、同時對反應條件(如溫度、pH等)有嚴格的選擇性外,醇對底物和反應類型也有嚴格的選擇性。如圖四所示:
|
|
| 圖四 反應特異性和底物特異性 |
根據酶對化學反應類型和底物分子結構選擇性的嚴格程度,酶的特異性可分為三種類型:
(1)絕對特異性(absolute specifity)&md
(2)相對特異性(relative specificity)——有一些酶的特異性相對較差,這些酶只能作用于一類化合物或一種化學鍵,如圖四中的B酶。這種不太嚴格的選擇性,稱為相對特異性。
(3)立體異構特異性(sterospecificity)——這類酶能辨別底物不同的立體異構體,只對其中一種構型起催化作用。包括旋光異構特異性和幾何異構特異性。
〈三)酶的活性中心(active center)或稱活性部(active site)
絕大多數酶是蛋白質,是由各種氨基酸分子以肽鍵連接的線狀大分子。由于分子中有-NH2、-COOH基團和各種側鏈,它們間存在著氫鍵、離子鍵和范德華等引力,少數酶有共價結合,如二硫鍵,致使蛋白質分子呈“線團”狀(三級結構-tertiary structure)。如圖五所示
|
|
| 圖五 |
酶的活性中心是酶和底物生成復合物、進而發生催化反應的部位。
在活性中心中,酶和底物可以通過各基團間的非共價結合,生成酶-底物復合物。如表1所示:
| 表1 酶和底物間的非共價鍵作用 |
|
|
對一個單純酶來說,活性中心是指在“線團”狀的酶蛋白結構外表面上相互靠近的一些氨基酸殘基或其殘基上的某些基團組成的區域。活性中心有兩類必需基團:―類是能與底物(和輔酶)結合形成酶-底物復合物的結合基團(binding group);另一類是影響底物中某些
此外,酶分子中還有一些其他基團,它們雖然沒有結合和催化功能,但能營造一個使酶的活性中心處于合適的空間構象,如產生凹穴或裂縫,誘導底物與必需基團接近和結合,有人稱它為誘導契合(induced fit),如圖六所示:
|
|
催化反應時,酶的活性中心先后進行:a.底物和酶靠近(approximation)、定位取向(orientation)誘導契合;b.排除表面溶劑化層,如水,使底物和酶更緊密接觸;c.過渡態的穩定化和d.基團轉移這四個過程。如圖七所示:
|
|
| 圖七 |
(四)酶的活力(activity)
酶的活力單位:
(1)國際單位(IU):
1961年國際酶學會(the international Union of Biochemistry)提出,I964年被采用。定義:1個酶活力單位是指在特定條件(
*注意:在國際度量衡(CGPM)中,SI)的時間單位是秒(s)不是分鐘(min)。
(2)Kata1單位(Kat):
由于上述矛盾,1978年國際度量衡(CGPM)推薦、1999年官方接受,用Katal為酶的活力單位,指在特定條件下、酶被底物飽和時,每秒鐘轉化1mo1底物所需的酶量,
1IU=1/6O μkatal=16.67n kata1
酶的比活力(specific activity):
每分鐘每毫克酶蛋白在
(3)轉換數(Turnover nunber)Kcat
在酶學中,定義單位時間、每個酶分子中活性部位能使底物轉換成產物的最大分子數,它可按下面的米-曼方程式, Kcat=Vmax/[E]T計算求得,式中[E]T為總(total)的酶濃度。
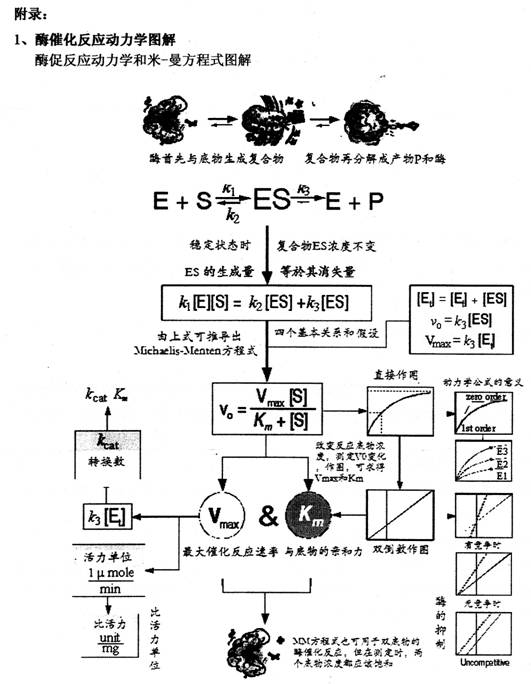
三、酶促反應動力學
酶促反應動力學是研究酶促反應速率以及各種因素對反應速率的影響。這些影響因素有:底物濃度、酶的濃度、pH、溫度、抑制劑以及激活劑等。
在酶促反應中,酶(E)首先與底物(S)生成“中間產物——酶-底物復合物(ES)”,然后這復合物再分解成產物(P)和游離的酶。
![]() (一)底物濃度[S]對酶促反應初始速率(V)的影響
(一)底物濃度[S]對酶促反應初始速率(V)的影響
(1)米-曼方程式(Michaelis-Menten Equation)和米-曼常數Km(Michaelis-Menten Constant)
l913年Leonor Michaelis和Maud L.Menten基于下列假設,推導出米-曼方程式,它表示底物濃度[s]變化對酶促反應初始速率(V)影響的方程式(方程式推導從略)。
這些假設是:(1)單底物反應;(2)測定的反應速率是初始速率(initial rate),困為反應剛剛開始,生成產物量極少,產物的逆反應可忽略不計;(3)在反應起始時,底物濃度[S]遠遠大于酶濃度[E],[S]變化可以忽略不計。
![]() V-不同底物濃度[S]時的初始速率
V-不同底物濃度[S]時的初始速率
Vmax ——最大初始反應速率
Km ——米-曼常數,是初始速率V為1/2 Vmax時的底物濃度[S]。
Kl、K2、k3分別為酶E和底物S生成復合物ES、復合物的逆反應和復合物分解生成產物和游離酶的三個速率常數
從米-曼方程式可推論出:
l、當底物濃度[S很低時,如[S]<<Km,式中分母Km+[S]≌Km,則V=Vmax/Km
2、如底物濃度[S]很高,且[S]>>Km,Km+[S]≌[S],則V≌Vmax,這時所有酶分子中的活性部位均被底物飽和。
3、當V=1/2 Vmax,代入方程式,得Km=[S],即表示當反應速率為最大速率的一半時,米-曼常數Km值等于底物濃度[S]。
(2)米曼常數(Km)
米-曼常數(Km)是酶的特征常數。在一定反應條件(溫度、pH和離子強度)下,它只與酶的種類和底物的性質有關,與酶的濃度無關。
如酶能催化幾種不同的底物,對每種底物都有一個特定的Km值,其中Km值最小的稱該酶的最適底物。Km值小,要達到反應速率為最大速率的一半時,所需的底物濃度[S]就低。
當復合物ES離解成E和S的速率K2遠遠大于ES分解成游離酶E和產物P的速率k3時,即K2>>K3,K2+Κ3≡Κ2,則
| Km= | | = | 復合物ES離解成E和S的速率常數 | =Ks(離解常數) |
| K1 | 酶和底物生成復合物ES的速率常數 |
此時Km表征酶與底物的親合力。但實際上,不是所有的酶促反應中,永遠是k2>>k3,所以Km和Ks(離解常數)不是同一個函義,不能相互取代使用。
Km值越大,酶與底物親合力越小,要達到最大速率的一半時所需底物濃度[S]越高:反之, Km值越小,酶與底物親合力越大,則要達到最大速率的一半時所需底物濃度[S]低。不同種類的酶,對特定的底物,有不同的Km值。對于一種未知的酶,可在規定的條件下測定其Km值加以鑒定。
(3)用作圖法測定求得酶的Vmax和Km
1、米-方程式曲線
|
|
| 圖八wxtu2lc is-nten ion |
如圖八所示,米-曼方程式的曲線由三部分組成:
第一部分:起始反應時的直線部分。此時反應速率和底物濃度[S]成正比,反應屬一級反應。
第二部分:提高底物濃度,使酶分子的活性部位逐步底物占有,圖形中部呈曲線,此時反應屬混合級反應。
第三部分:當底物濃度很高,使所有的酶分子的活性部位均被底物占有和飽和。此時,再增加底物濃度,反應速率保持不變,成漸近線,反應屬零級反應。
2、Lineweaveer-Burg(簡稱林-貝)雙倒數法(double reciprocal plot)作圖求Km值和Vmax。
理論上,可以用多種方法測定米-曼常數Km和Vmax值。例如,在反應中固定酶的濃度,測定在不同底物濃度下的初始反應速率,求得Km和Vmax值。但是由于米-曼方程式曲線在接近Vmax時是漸近過程,很難測得真實的Vmax,所以不能直接用起始速率對底物濃度作圖來求得Km或Vmax值。
1930年Lineweaver和Burk把米-曼方程式兩邊取倒數,即得下式。此式表示1/V和1/[S]呈直線關系,式中,Km/Vmax是斜率,1/Vmax是y軸上的截距。
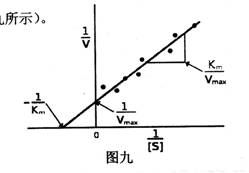
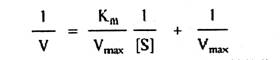 將1/V對l/[S]作圖,即可得到一條直線。該直線在Y軸的截距為1/Vmax,在X軸上的截距為-1/Km的絕對值(如圖九所示)。
將1/V對l/[S]作圖,即可得到一條直線。該直線在Y軸的截距為1/Vmax,在X軸上的截距為-1/Km的絕對值(如圖九所示)。
 (二)在底物濃度足夠大時,反應速率隨酶濃度提高而呈直線增加
(二)在底物濃度足夠大時,反應速率隨酶濃度提高而呈直線增加
當反應體系中,底物濃度很高,且大大超過酶濃度,酶分子中所有活性部位都與底物生成復合物ES,且被底物飽和時,反應速率(V=K3[ES]=K3[E])達到最大值Vmax。此時,反應屬一級反應,即反應速率與酶濃度增加成正比的直線關系,如圖十所示。
|
|
| 圖十 酶濃度對速率作圖 |
三)溫度對酶促反應速率影響的雙重性
酶是生物催化劑,溫度對酶促反應有雙重影響。升高溫度一方面可以加怏酶促反應速率。但是,因為大多數酶是蛋白質大分子,常態下,因分子鏈中各種基團的相互吸引,使酶蛋白構象呈穩定的“線團”狀,而活性中心就在其線團的凹穴表面。提高溫度會破壞基團間的相互吸引,嚴重時會使酶變性失活,所以過分提高溫度反會使酶變性失活,并不可逆轉。
大多數酶在溫度
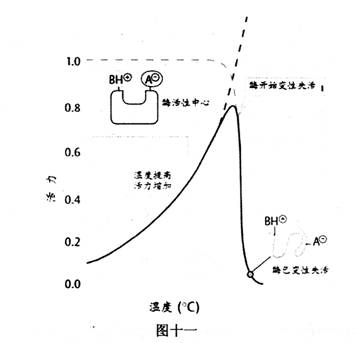 酶的最適溫度不是酶的特性常數,因為它隨反應進行的時間有關。酶可以在較短時間內承受較高的溫度。相反,隨著反應時間延長,最適反應溫度也會降低。低溫雖會降低酶的活性,但不會破壞酶,在溫度回升后,酶的活性又會恢復。
酶的最適溫度不是酶的特性常數,因為它隨反應進行的時間有關。酶可以在較短時間內承受較高的溫度。相反,隨著反應時間延長,最適反應溫度也會降低。低溫雖會降低酶的活性,但不會破壞酶,在溫度回升后,酶的活性又會恢復。
(四)pH對酶促反應速率的影響
酶蛋白是兩性的高分子電解質,在不同pH條件下,酶分子的酸性基團和堿性基團將發生不同的離解〈特別是處于活性中心的基團),只有當這些基團處于一定的離解狀態下,才對底物有最大的親和力。同時pH也會改變某些底物(蛋白質、氨基酸等)和輔酶的離解程度,從而影響它們與酶和底物的結合。
大多數酶的活力都會受環境pH的影響。只有在某一pH時,酶的反應速率最大,這是酶的最適pH(optimum pH)。高于或低于此pH,反應速率下降。如圖十二所示
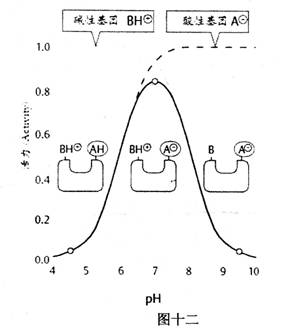 最適pH會隨底物種類、濃度和緩沖體系不同而不同,而且常與酶的等電點不一致。因此最適pH不是酶的特征常數,只有在一定條件下才有意義。pH過低或過高
最適pH會隨底物種類、濃度和緩沖體系不同而不同,而且常與酶的等電點不一致。因此最適pH不是酶的特征常數,只有在一定條件下才有意義。pH過低或過高
(五)抑制劑和激活劑對反應速度的影咱
(1)抑制劑
一些能與酶的必需基團相結合,從而抑制酶的催化活性但不引起酶蛋白變性的物質統稱為酶的抑制劑(inhibitor)。根據抑制劑與酶活性中心的必需基團結合的緊密程度,抑制劑分為不可逆性抑制(irreversible inhibition)和可逆性抑制作用(reversible inhibition)
1)、不可逆性抑制(irreversible inhhibiton)
抑制劑與酶活性中心的必需基團共價結合, 使酶失活,且此抑制劑不能用透析、超濾等方法予以去除。
2)、可逆性抑制作用(reversible inhibition)
這類抑制劑通常以非共價與酶和(或)酶-底物復合物可逆性結合,使酶活性降低或消失。采用透析或超濾的方法可將抑制劑除去。這類可逆性抑制作用又可分為三種類型:競爭性抑制作用、非競爭性抑制作用和反競爭性抑制作用。
(2)、激活劑(activator)
能使無活性酶轉變為有活性或使酶活性增加的物質稱為酶的激活劑。激活劑大多為金屬離子,如Mg2+,K+,Mn2+等,少數為陰離子,如Cl-等。也有許多有機化合物激活劑,如膽汁酸鹽等。激活劑對酶的作用有一定選擇性,按其對酶促反應的需要程度,激活劑又可分為必需激活劑(essential activator)和非必需激活劑 (non-essential activator)
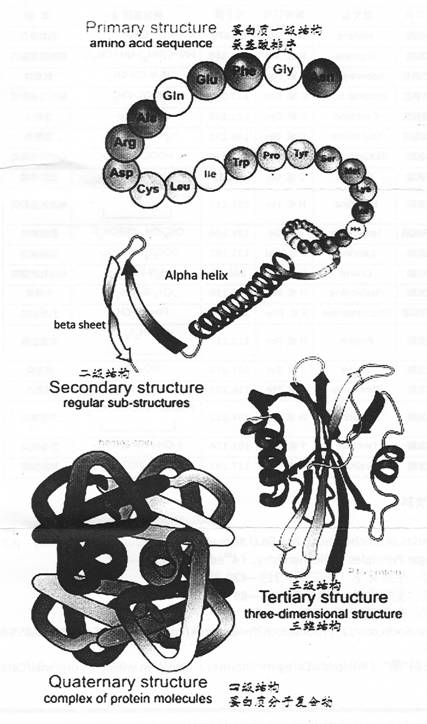
 2、蛋白質結構圖
2、蛋白質結構圖
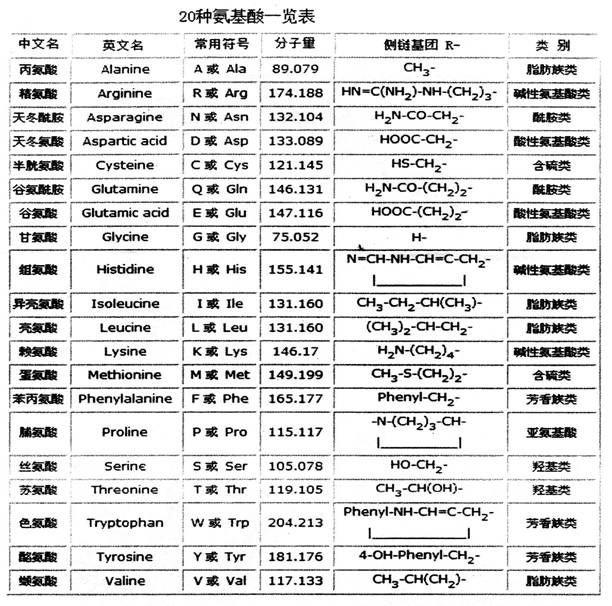
 3)20種氨基酸
3)20種氨基酸
 相關信息
相關信息 






 推薦企業
推薦企業 推薦企業
推薦企業
 推薦企業
推薦企業